
News information
分類:行業資訊 發布時間:2024-05-16 訪問量:751
仿制藥參比制劑是指用于仿制藥質量和療效一致性評價的對照藥品,通常為被仿制的對象,如原研藥品或國際公認的同種藥物。參比制劑應為處方工藝合理、質量穩定、療效確切的藥品。
仿制藥是指與被仿制藥具有相同的活性成分、劑型、給藥途徑和治療作用的藥品。原研藥品是指境內外首個獲準上市,且具有完整和充分的安全性、有效性數據作為上市依據的藥品。國際公認的同種藥物是指在歐盟、美國、日本獲準上市并獲得參比制劑地位的仿制藥。
進行仿制藥質量和療效一致性評價,就是要求對已經批準上市的仿制藥品,在質量和療效上與原研藥能夠一致,在臨床上與原研藥可以相互替代,這樣有利于節約社會的醫藥費用。如需更多關于仿制藥參比制劑的信息,建議查閱相關藥品法規或咨詢藥品專家。
參比制劑有什么要求
參比制劑在仿制藥質量和療效一致性評價中扮演著重要角色,它通常是原研藥品或國際公認的同種藥物,用于作為仿制藥質量和療效的對照。以下是參比制劑的一些主要要求:
優先選擇:優先選擇原研上市許可持有廠家原產地進口產品。如果原研藥品未在國內上市或不符合參比制劑條件,可以選擇國際公認同種藥物作為參比制劑。
質量和療效:參比制劑應為處方工藝合理、質量穩定、療效確切的藥品。其安全性和有效性應有充分的數據支持。
證明文件:如果參比制劑由企業自行購買,應有合法證明文件。在境外購買的參比制劑,應提供辦理一次性進口所需的《進口藥品批件》。
可獲得性:參比制劑的批次和數量應滿足企業自身研究及藥品檢驗機構復核檢驗的需要。
與原研藥品的一致性:如果選用的是地產化藥品作為參比制劑,原研企業應能證明其地產化藥品與原研藥品在質量、療效等方面的一致性。
國際公認性:如果原研藥品未在國內上市,可以選擇在歐盟、美國、日本上市并獲得參比制劑地位的仿制藥作為參比制劑。
這些要求旨在確保參比制劑的質量、療效和可獲得性,從而確保仿制藥的質量和療效與原研藥品一致,為患者提供安全、有效的治療選擇。
參比制劑和對比制劑有什么區別
參比制劑和對比制劑在醫藥領域中具有不同的含義和用途。
參比制劑(Reference Listed Drug, RLD)主要用于仿制藥的質量和療效一致性評價,作為對照藥品,它通常是原研藥品或國際公認的同種藥物。參比制劑應為處方工藝合理、質量穩定、療效確切的藥品。在仿制藥研發過程中,參比制劑的選擇至關重要,因為它為仿制藥提供了質量和療效的基準。
而對比制劑(Contrast Agent)則主要用于醫學影像檢查中,通過人為地將某種物質引入器官內部或其周圍以增加其對比,從而幫助醫生更清晰地觀察器官結構和病變情況。對比劑按原子量和比重可分為陽性對比劑和陰性對比劑。陽性對比劑如鋇劑和碘制劑,而陰性對比劑則是原子量小、比重低的物質,如各種氣體。
綜上所述,參比制劑和對比制劑在醫藥領域中的用途不同。參比制劑主要用于仿制藥的質量和療效一致性評價,而對比制劑則用于醫學影像檢查中幫助醫生觀察器官結構和病變情況。
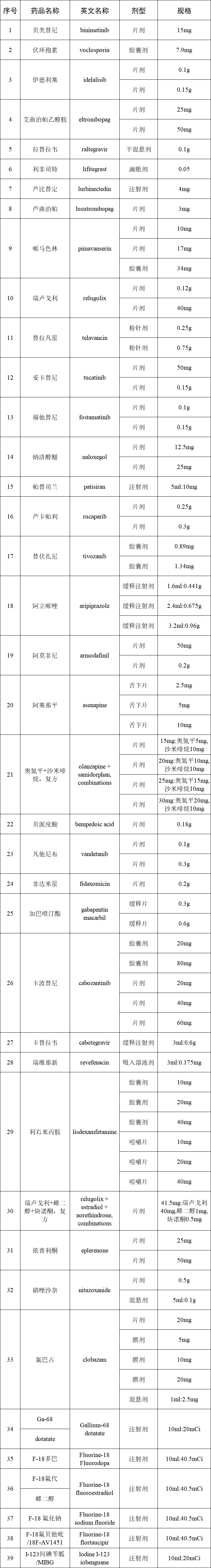

國家醫保部門從多個方面考慮到參保人員的利益,進而對相關政策進行調整和完善,提升居民的生活幸福感。
2020年-2025年,因新品上市以及患癌人數不斷增加,因此從市場規模也隨之上升。根據頭豹研究院整理,ADC藥物的市場規模預計在2024年有望達到74 億元,2030年預計市場規模達到292億元人民幣,2024-2030年復合增長率為25.71%。?

國家衛生健康委發布最新公告顯示,2020年各類傳播途徑的甲乙類傳染病發病率均呈現明顯下降,其中腸道傳染病發病率較2019年下降29.4%、呼吸道傳染病發病率較2019年下降12.9%。因此,全球,包括中國在內的抗菌藥物的使用額呈下降趨勢。
隨著新藥的不斷研發和政策的完善,漸凍癥治療市場有望迎來更加廣闊的發展前景。